服務(wù)導(dǎo)航
國家出手!口罩出口新規(guī)!附CE/FDA認(rèn)證資格認(rèn)證指南
來源: 時(shí)間:2020-04-02
商務(wù)部:4月1日起!出口醫(yī)療物資出新規(guī)


商務(wù)部昨晚發(fā)布公告:在疫情防控特殊時(shí)期,為有效支持全球抗擊疫情,保證產(chǎn)品質(zhì)量安全、規(guī)范出口秩序,自4月1日起,出口新型冠狀病毒檢測試劑、醫(yī)用口罩、醫(yī)用防護(hù)服、呼吸機(jī)、紅外體溫計(jì)的企業(yè)向海關(guān)報(bào)關(guān)時(shí),須提供書面或電子聲明(模版見附件1),承諾出口產(chǎn)品已取得我國醫(yī)療器械產(chǎn)品注冊證書(相關(guān)注冊信息見附件2),符合進(jìn)口國(地區(qū))的質(zhì)量標(biāo)準(zhǔn)要求。海關(guān)憑藥品監(jiān)督管理部門批準(zhǔn)的醫(yī)療器械產(chǎn)品注冊證書驗(yàn)放。上述醫(yī)療物資出口質(zhì)量監(jiān)管措施將視疫情發(fā)展情況動(dòng)態(tài)調(diào)整。
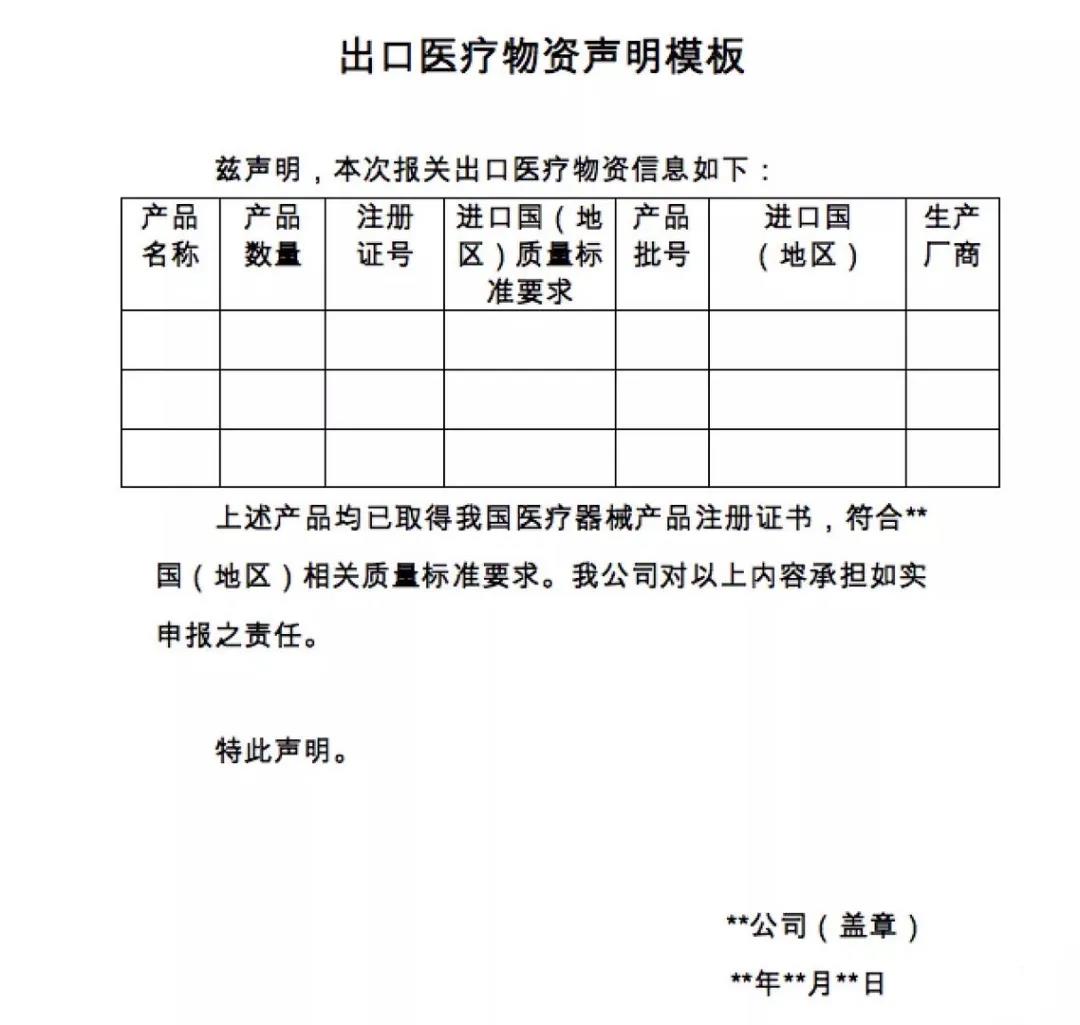
▲出口報(bào)關(guān)時(shí)新增的申明模板
根據(jù)國家商務(wù)部,海關(guān)總署和國家藥品監(jiān)督管理局官方公布的已經(jīng)取得我國醫(yī)療器械產(chǎn)品注冊證書的合格企業(yè),全國共計(jì)2047家!
大家在詢價(jià),采購和出口時(shí),可以仔細(xì)從中查找你的供應(yīng)商是否在三個(gè)部委公布的合規(guī)清單里面!
避免采購劣質(zhì)產(chǎn)品,導(dǎo)致貨物被查被扣并最終血本無歸!
一次性使用醫(yī)用口罩(共752家)
醫(yī)用防護(hù)口罩(共150家)
醫(yī)用外科口罩(共523家)
醫(yī)用防護(hù)服(共301家)
醫(yī)用防護(hù)口罩(共23家)
呼吸機(jī)(共62家)
紅外體溫計(jì)(共236家)
歐盟CE認(rèn)證資格
隨著新冠肺炎疫情的迅速蔓延,意大利、法國、德國等國紛紛淪陷,歐洲成為了疫情重災(zāi)區(qū)。在防控疫情的過程中,由于醫(yī)用口罩、防護(hù)服等醫(yī)護(hù)物資的嚴(yán)重短缺,歐洲對外釋放了巨大的防護(hù)用品需求。目前,中國已經(jīng)取得了新冠防疫的階段性勝利,作為世界上最大的醫(yī)用防護(hù)用品生產(chǎn)國,無論是傳統(tǒng)醫(yī)療生產(chǎn)企業(yè),還是決定踏入這一陌生領(lǐng)域的新企業(yè),都決定將多余的產(chǎn)能利用起來,將此類產(chǎn)品銷往歐洲市場。
出口歐盟市場,CE認(rèn)證必不可少。目前市場上出現(xiàn)了各色各樣的醫(yī)療CE證書,讓人眼花繚亂。在各種行業(yè)微信群里,經(jīng)常可以看到有人發(fā)出一張所謂的CE證書,請大家?guī)兔Ρ鎰e真?zhèn)巍榱烁玫貛椭酱蠹遥旅嫖覀兙蛠碚務(wù)劸唧w的鑒別方法。
查詢CE證書的真?zhèn)危卸喾N方式,首先是最簡單粗暴的一種。大的公告機(jī)構(gòu)會(huì)在自己的官網(wǎng)上開放查詢證書的窗口,當(dāng)然,這種方式僅適用于發(fā)證機(jī)構(gòu)正好提供了查詢服務(wù)的情況。而對于未開放證書查詢服務(wù)的機(jī)構(gòu),就不會(huì)奏效了。那么對于此類情況,當(dāng)我們拿到一張醫(yī)療CE證書時(shí),我們又該如何鑒別呢?
歐盟官網(wǎng)MDD 93/42/EEC醫(yī)療器械指令授權(quán)的機(jī)構(gòu)查詢地址:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=13
歐盟官網(wǎng)MDR (EU) 2017/745醫(yī)療器械法規(guī)授權(quán)的機(jī)構(gòu)查詢地址:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=34
歐盟官網(wǎng) (EU)2016/425個(gè)人防護(hù)裝備授權(quán)的機(jī)構(gòu)查詢地址:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=15550

自2020年5月26日起,MDR (EU) 2017/745醫(yī)療器械法規(guī)將正式取代歐盟現(xiàn)行的MDD醫(yī)療器械指令強(qiáng)制實(shí)施,同樣在歐盟官網(wǎng)可以查詢到,擁有MDR授權(quán)的公告機(jī)構(gòu)目前只有12家。
所以,如果您手上的醫(yī)療CE證書發(fā)證機(jī)構(gòu)不在以上名單范圍內(nèi),則說明它并不具備醫(yī)療產(chǎn)品的歐盟發(fā)證資質(zhì),更別談CE證書的發(fā)放了,那么,很遺憾地說,您拿到的這張“”CE證書“是無效的。
另外,我們也可以從醫(yī)療器械產(chǎn)品CE認(rèn)證的流程著手去分析,完成鑒別。

美國FDA
510(k)的申請流程如下:

通常一個(gè)產(chǎn)品從啟動(dòng)510(k),準(zhǔn)備測試和各類文件,直至最終的審核結(jié)束,需要?dú)v經(jīng)8-10個(gè)月,而初次申請的企業(yè),這個(gè)時(shí)間通常會(huì)更長。
除了510(k)以外,F(xiàn)DA要求所有的醫(yī)療器械企業(yè)都需要進(jìn)行場所注冊(Establishment Registration)和產(chǎn)品列示(Product Listing),這一要求對于應(yīng)急使用授權(quán)的產(chǎn)品也不例外。對于所有的海外企業(yè),在進(jìn)行場所注冊之前應(yīng)先獲得鄧白氏編碼,編碼在中國由華夏鄧白氏公司代理發(fā)放,免費(fèi)的代碼需要大約30天可以獲得。獲取鄧白氏編碼后,大約需要1-2周左右完成場所注冊和產(chǎn)品列示。
無論是510(k),場所注冊或者產(chǎn)品列示,F(xiàn)DA都不會(huì)向企業(yè)頒發(fā)任何證書,僅以美國FDA數(shù)據(jù)庫中的數(shù)據(jù)為準(zhǔn)。也就是說,大家見過的各種有著老鷹標(biāo)記的證書都是沒有任何效力的。
目前,新冠疫情在美國呈現(xiàn)明顯爆發(fā)的趨勢,各類醫(yī)療物資也趨于緊張。美國食品藥品監(jiān)督管理局(FDA)早在今年(2020年)2月初就開始對醫(yī)療器械潛在短缺的情況進(jìn)行調(diào)查,為了應(yīng)對各類醫(yī)療器械的緊缺FDA發(fā)布了各類應(yīng)急使用授權(quán)(Emergency Use Authorization,EUA)。目前可以申請EUA的產(chǎn)品主要是未獲上市的N95口罩、未獲上市的新冠病毒診斷試劑、未獲上市的酒精洗手液產(chǎn)品、已上市但需擴(kuò)展用途的非侵入遠(yuǎn)程監(jiān)護(hù)系統(tǒng)、已上市和未上市的呼吸設(shè)備。
新冠檢測試劑:首當(dāng)其沖的就是診斷試劑,F(xiàn)DA已經(jīng)就該產(chǎn)品發(fā)布了第二版的指導(dǎo)原則。第一版指導(dǎo)原則主要針對美國國內(nèi)臨床實(shí)驗(yàn)室自我開發(fā)的檢驗(yàn)方法的EUA申請,而第二版則納入了針對生廠商的遞交EUA申請的詳細(xì)指導(dǎo)。EUA的申請要包含的內(nèi)容與510(k)相似,需要提交檢測試劑的描述、預(yù)期用途、性能評價(jià)報(bào)告、臨床評價(jià)方案、穩(wěn)定性試驗(yàn)方案、標(biāo)簽標(biāo)識(shí)等。由于屬于應(yīng)急審批,F(xiàn)DA還要求企業(yè)必須提供針對患者和專業(yè)人員的明白紙(Fact Sheet)。目前海河咨詢已經(jīng)完成了新冠病毒膠檢測試劑盒膠體金法的EUA申請。
(2)經(jīng)NIOSH批準(zhǔn)但已過制造商推薦的保存期限的過濾面罩口罩,供醫(yī)護(hù)人員在醫(yī)療環(huán)境中使用,以防止醫(yī)護(hù)人員由于面罩口罩短缺,而暴露于病原性生物空氣傳播顆粒中。
考慮到這樣的措施還是無法保障美國市場的口罩供應(yīng),F(xiàn)DA又在近期發(fā)布口罩的EUA申請,特別地,沒有獲得NIOSH批準(zhǔn)的口罩也可以進(jìn)行EUA的申請,但是必須符合:
條件1-滿足特定國家/地區(qū)性能標(biāo)準(zhǔn),包括
澳大利亞:P2,P3
巴西:PFF2,PFF3
歐盟:FFP2,F(xiàn)FP3
日本:DS/DL3,DS/DL2
韓國:Special 1st
墨西哥:N100, P100, R100, N99, P99, R99, N95, P95, R95
條件2-獲得特定國家上市許可,包括:
歐盟:CE認(rèn)證;
澳大利亞:ARTG注冊
加拿大:注冊證;
日本:醫(yī)療器械注冊證。
酒精洗手液產(chǎn)品:之前酒精洗手液產(chǎn)品在美國是按照非處方類藥品進(jìn)行管理的,洗手液中的酒精則是按照API進(jìn)行管理的。目前,F(xiàn)DA已經(jīng)發(fā)布通知,不會(huì)對提供用于洗手液的酒精的生產(chǎn)商或者洗手液的生產(chǎn)商采取行動(dòng),即可以認(rèn)為,F(xiàn)DA將允許用于洗手液的酒精和基于酒精的洗手液在滿足限定條件下直接在美國銷售。海河咨詢特別提醒:對于洗手液的生產(chǎn)商僅限定適用于藥劑師以及聯(lián)邦設(shè)施,不適用于其他商業(yè)生產(chǎn)商。
★ 口罩出口--海關(guān)技術(shù)性貿(mào)易措施指南 ★
一、出口通關(guān)提示
1.報(bào)關(guān)前提條件
收發(fā)貨人注冊編碼(慈善機(jī)構(gòu)可為臨時(shí)編碼),需辦理無紙化通關(guān)法人卡
2.出口資質(zhì)
口罩出口對生產(chǎn)銷售單位、境內(nèi)發(fā)貨人,除滿足國內(nèi)生產(chǎn)、市場流通資質(zhì)需求外,中國海關(guān)無特殊資質(zhì)要求。
3.出口申報(bào)要求
(1)商品歸類:除特殊情況外,絕大部分口罩應(yīng)歸入稅號63079000。
(2)檢驗(yàn)檢疫:口罩為非法檢產(chǎn)品,申報(bào)時(shí)檢驗(yàn)檢疫項(xiàng)目無需填報(bào)。根據(jù)我國政府與相關(guān)國家簽訂的政府間檢驗(yàn)協(xié)議,對出口伊朗等少數(shù)幾個(gè)國家的產(chǎn)品需按規(guī)定進(jìn)行裝運(yùn)前檢驗(yàn)。
(3)關(guān)稅征免:如出口物資為貿(mào)易性質(zhì),征免性質(zhì)申報(bào)一般征稅,征免方式申報(bào)照章征稅;如為捐贈(zèng)性質(zhì),境內(nèi)發(fā)貨人為貿(mào)易代理商、慈善機(jī)構(gòu)等,征免性質(zhì)可不填,征免方式申報(bào)全免。
(4)禁限管理:目前商務(wù)部未對口罩設(shè)置貿(mào)易管制要求,中國海關(guān)也無針對防護(hù)物資的監(jiān)管證件口岸驗(yàn)核要求。
(5)申報(bào)規(guī)范:按照規(guī)范申報(bào)要求填寫商品名稱、成分含量;如物資非中國生產(chǎn),原產(chǎn)國按照實(shí)際生產(chǎn)國填寫。
4.出口退稅
口罩的出口退稅率為13%。
5.中美關(guān)稅排除加征
美國企業(yè)可申請排除口罩進(jìn)口加征關(guān)稅,但是目前只有少數(shù)企業(yè)獲準(zhǔn)豁免。詳見美國貿(mào)易代表辦公室網(wǎng)站https://ustr.gov/。
6.快速通關(guān)保障
物資出口申報(bào)如遇單窗等系統(tǒng)故障,可聯(lián)系現(xiàn)場海關(guān)采取應(yīng)急方式處置,或者撥打海關(guān)12360熱線進(jìn)行咨詢。
*以下內(nèi)容是根據(jù)國內(nèi)外相關(guān)政府機(jī)構(gòu)、專業(yè)網(wǎng)站、新聞報(bào)道,收集整理而成,僅供參考。具體內(nèi)容以相關(guān)管理部門、國外官方機(jī)構(gòu)要求為準(zhǔn)。
二、出口前準(zhǔn)備
1.明確口罩分類
國外按照用途一般分為個(gè)人防護(hù)和醫(yī)用兩類口罩,國內(nèi)出口貿(mào)易企業(yè)需具備的資質(zhì)和材料如下:
(1)營業(yè)執(zhí)照(經(jīng)營范圍有相關(guān)經(jīng)營內(nèi)容)。
(2)企業(yè)生產(chǎn)許可證(生產(chǎn)企業(yè))。
(3)產(chǎn)品檢驗(yàn)報(bào)告(生產(chǎn)企業(yè))。
(4)醫(yī)療器械注冊證(非醫(yī)用不需要)。
(5)產(chǎn)品說明書(跟著產(chǎn)品提供)、標(biāo)簽(隨附產(chǎn)品提供)。
(6)產(chǎn)品批次/號(外包裝)。
(7)產(chǎn)品質(zhì)量安全書或合格證(跟著產(chǎn)品提供)。
(8)產(chǎn)品樣品圖片及外包裝圖片。
(9)貿(mào)易公司須取得海關(guān)收發(fā)貨人注冊備案。
2.國內(nèi)出口口罩生產(chǎn)企業(yè)資質(zhì)證明
生產(chǎn)個(gè)人防護(hù)或者工業(yè)用非醫(yī)療器械管理的普通口罩,有進(jìn)出口權(quán)的企業(yè),可自行直接出口。
生產(chǎn)屬于醫(yī)療器械管理的口罩用于出口,中國海關(guān)不需要企業(yè)提供相關(guān)資質(zhì)證明文件,但一般進(jìn)口國會(huì)要求生產(chǎn)企業(yè)提供產(chǎn)品三證,以證明該進(jìn)口的商品在中國已合法上市,具體如下:
(1)營業(yè)執(zhí)照(經(jīng)營范圍包含有醫(yī)療器械相關(guān),非醫(yī)療級別的物品不需要)。
(2)醫(yī)療器械產(chǎn)品備案證或者注冊證。
(3)廠家檢測報(bào)告。
生產(chǎn)企業(yè)有進(jìn)出口權(quán),可以自行出口,如沒有進(jìn)出口權(quán),可以通過外貿(mào)代理進(jìn)行出口銷售。
3.內(nèi)貿(mào)企業(yè)做出口需要取得的基本資質(zhì)
(1)向市場監(jiān)管部門取得營業(yè)執(zhí)照,增加經(jīng)營范圍“貨物進(jìn)出口、技術(shù)進(jìn)出口、代理進(jìn)出口”。
(2)向商務(wù)部門取得進(jìn)出口權(quán),可直接在商務(wù)部業(yè)務(wù)系統(tǒng)統(tǒng)一平臺(tái)(http://iecms.mofcom.gov.cn/)申請,網(wǎng)上提交材料。
(3)向外匯管理局申請取得開設(shè)外匯賬戶許可。
(4)辦理進(jìn)出口貨物收發(fā)貨人海關(guān)注冊登記。
三、各國口罩準(zhǔn)入條件(產(chǎn)品準(zhǔn)入條件)
1.美國
必要資料:提單,箱單,發(fā)票。
個(gè)人防護(hù)口罩:必須取得美國 NIOSH檢測認(rèn)證,即National Institute for Occupational Safety and Health美國國家職業(yè)安全衛(wèi)生研究所認(rèn)證。
醫(yī)用口罩:須取得美國FDA注冊許可。
2.歐盟
必要資料:提單,箱單,發(fā)票。
個(gè)人防護(hù)口罩:個(gè)人防護(hù)口罩的歐盟標(biāo)準(zhǔn)是EN149,按照標(biāo)準(zhǔn)將口罩分為FFP1/FFP2和FFP3三個(gè)類別。所有出口歐盟的口罩必須獲得CE認(rèn)證證書。CE認(rèn)證是歐盟實(shí)行的強(qiáng)制性產(chǎn)品安全認(rèn)證制度,目的是為了保障歐盟國家人民的生命財(cái)產(chǎn)安全。
醫(yī)用口罩:醫(yī)用口罩對應(yīng)的歐盟標(biāo)準(zhǔn)是EN14683。
產(chǎn)品在歐盟銷售需要出具歐盟自由銷售證書 Free Sale Certificate,有了CE標(biāo)志并進(jìn)行了相關(guān)指令中要求的歐盟注冊后,中國的制造商出口歐盟不需要自由銷售證書。
3.日本
必要資料:提單,箱單,發(fā)票,日本國外的制造商必須向PMDA注冊制造商信息。
口罩包裝要求:包裝上印有ウィルスカット(中文翻譯:病毒攔截)99%的字樣
PFE:0.1um微粒子顆粒過濾效率
BFE:細(xì)菌過濾率
VFE:病毒過濾率
口罩品質(zhì)標(biāo)準(zhǔn):
(1)醫(yī)用防護(hù)口罩:符合中國GB 19083-2010 強(qiáng)制性標(biāo)準(zhǔn),過濾效率≥95%(使用非油性顆粒物測試)。
(2) N95口罩:美國NIOSH認(rèn)證,非油性顆粒物過濾效率≥95%。
(3) KN95口罩:符合中國GB 2626 強(qiáng)制性標(biāo)準(zhǔn),非油性顆粒物過濾效率≥95%。
4.韓國
必要資料:提單,箱單,發(fā)票,韓國進(jìn)口商營業(yè)執(zhí)照。
個(gè)人防護(hù)口罩標(biāo)準(zhǔn):KF (Korean filter) 系列分為KF80、KF94、KF99
執(zhí)行標(biāo)準(zhǔn)規(guī)范:MFDS Notice No. 2015-69
韓國醫(yī)療器械準(zhǔn)入的法規(guī)門檻,基本分類為I、II、III、IV類,持證為韓國公司(License holder),韓國收貨人需要到韓國藥監(jiān)局Korea Pharmaceutical Traders Association. 提前備案進(jìn)口資質(zhì)(沒有不行)網(wǎng)址:www.kpta.or.kr。
5.澳大利亞
必要資料:提單,箱單,發(fā)票。
須通過澳洲的TGA注冊,符合標(biāo)準(zhǔn)規(guī)范:AS/NZS 1716:2012,此規(guī)范是澳大利亞和新西蘭的呼吸保護(hù)裝置標(biāo)準(zhǔn)。
TGA 是Therapeutic Goods Administration的簡寫,全稱是治療商品管理局,它是澳大利亞的治療商品(包括藥物、醫(yī)療器械、基因科技和血液制品)的監(jiān)督機(jī)構(gòu)。澳大利亞對醫(yī)療器械分為I類,Is and Im, IIa, IIb, III類,產(chǎn)品的分類幾乎和歐盟分類一致,如果產(chǎn)品已經(jīng)獲得CE標(biāo)志,則產(chǎn)品類別可以按照CE分類。
四、各國注冊、認(rèn)證簡要辦理流程
1.美國NIOSH認(rèn)證
需按照NIOSH的指南實(shí)施,企業(yè)需寄送樣品至NIOSH實(shí)驗(yàn)室實(shí)施測試,同時(shí)提交技術(shù)性資料(包括質(zhì)量體系部分資料)至NIOSH文審,只有文審和測試都通過,NIOSH才核發(fā)批文。NIOSH將其認(rèn)證的防顆粒物口罩分為9類,具體的測試則由NIOSH下屬的NPPTL (National Personal Protective Technology Laboratory)實(shí)驗(yàn)室操作。主要測試指標(biāo)包括呼氣阻力測試、呼氣閥泄漏測試、吸氣阻力測試、過濾效率測試。
2.美國FDA注冊

3.歐盟CE注冊

4.日本PMDA注冊

(1)準(zhǔn)備階段。確定產(chǎn)品分類(I,II特殊控制,II類控制,III,IV)和產(chǎn)品JMDN編碼,選擇MAH(日本持證方);
(2)制造商向PMDA注冊工廠;
(3)II類特殊控制產(chǎn)品向授權(quán)認(rèn)證機(jī)構(gòu)PCB申請QMS工廠審核,其他II類產(chǎn)品和III類IV類產(chǎn)品向PMDA申請QMS工廠審核,并獲得QMS證書;
(4)申請Pre-Market Apporval證書,II類特殊控制由PCB發(fā)證,其他II類產(chǎn)品和III類IV類產(chǎn)品控制由MHLW(厚生勞動(dòng)省)發(fā)證;
(5) 支付申請費(fèi)用;
(6) 注冊文件整改,注冊批準(zhǔn);
(7)所有類別產(chǎn)品均需要MAH向RBHW(厚生省地區(qū)機(jī)構(gòu))進(jìn)行進(jìn)口通報(bào)注冊后才能進(jìn)口銷售。
5.韓國KFDA注冊
韓國衛(wèi)生福利部(MinistryofHealthandWelfare,MHW),簡稱衛(wèi)生部,主要負(fù)責(zé)管食品、藥品、化妝品和醫(yī)療器械的管理,是最主要的衛(wèi)生保健部門。依照《醫(yī)療器械法》,韓國衛(wèi)生福利部下屬的食品藥品安全部負(fù)責(zé)對醫(yī)療器械的監(jiān)管工作。KFDA注冊流程為:
(1)確定產(chǎn)品分類(I,II,III,IV),選擇KLH(韓國持證方);
(2)II類產(chǎn)品需申請KGMP證書和接受現(xiàn)場審核,II類產(chǎn)品一般是授權(quán)的第三方審核員,并獲得KGMP證書;
(3)II類產(chǎn)品需要送樣品到韓國MFDS授權(quán)的實(shí)驗(yàn)室進(jìn)行韓國標(biāo)準(zhǔn)的測試;
(4)由KLH向MFDS(韓國食品藥品安全部)提交技術(shù)文件(檢測報(bào)告,KGMP證書等),進(jìn)行注冊審批;
(5)支付申請費(fèi)用;
(6)注冊文件整改,注冊批準(zhǔn);
(7)指定韓國代理商和經(jīng)銷商,產(chǎn)品銷售。
6.澳大利亞TGA注冊
依據(jù)Australian Therapeutic Goods (Medical Devices) Regulations 2002,澳大利亞對醫(yī)療器械分為I類,Is and Im, IIa, IIb, III類,產(chǎn)品的分類幾乎和歐盟分類一致,如果產(chǎn)品已經(jīng)獲得CE標(biāo)志,則產(chǎn)品類別可以按照CE分類。如果已經(jīng)獲得歐盟公告機(jī)構(gòu)(Notified Body)簽發(fā)的CE證書,是可以被TGA認(rèn)可的,并可以作為滿足澳大利亞安全法規(guī)的重要注冊資料。

五、各國口罩技術(shù)標(biāo)準(zhǔn)對比(供生產(chǎn)企業(yè)參考)



六、各國口罩技術(shù)標(biāo)準(zhǔn)(供生產(chǎn)企業(yè)參考)
|
序號 |
標(biāo)準(zhǔn)號 |
標(biāo)準(zhǔn)名稱 |
狀態(tài) |
發(fā)布時(shí)間 |
|
國際 |
ISO 22609:2004 |
傳染試劑防護(hù)服.醫(yī)療面罩.防人造血滲透的試驗(yàn)方法(固定容積,水平注射) |
現(xiàn)行 |
2004/12/3 |
|
歐盟 |
EN 136-1998 |
呼吸保護(hù)裝置.全面罩.要求,試驗(yàn),標(biāo)記。 |
現(xiàn)行 |
1998/1/1 |
|
EN 140-1998+AC-1999 |
呼吸保護(hù)裝置.半面罩和四分之一面罩.要求,試驗(yàn)和標(biāo)記。 |
現(xiàn)行 |
1998/9/1 |
|
|
EN 143-2000 |
呼吸防護(hù)裝置.微粒過濾器.要求,試驗(yàn),標(biāo)記。 |
現(xiàn)行 |
2000/2/1 |
|
|
EN 149-2001 |
呼吸防護(hù)裝置.顆粒防護(hù)用過濾半面罩.要求,檢驗(yàn)和標(biāo)記。 |
現(xiàn)行 |
2001/4/1 |
|
|
EN 529-2005 |
呼吸保護(hù)裝置.選擇,使用,保養(yǎng)和維修的建議。 |
現(xiàn)行 |
2005 |
|
|
EN 12942-1998 |
呼吸保護(hù)器.帶全面罩,半面罩和四分之一面罩的鼓風(fēng)過濾裝置.要求,檢驗(yàn),標(biāo)識(shí)。 |
現(xiàn)行 |
1998 |
|
|
EN 14387-2004+A1-2008 |
呼吸保護(hù)裝置.氣體過濾器和組合過濾器.要求、測試、標(biāo)記。 |
現(xiàn)行 |
2004/1/1 |
|
|
EN 14683-2019 |
醫(yī)用口罩 要求和試驗(yàn)方法。 |
現(xiàn)行 |
2019/3/1 |
|
|
美國 |
ASTM F1862/F1862M-2017 |
醫(yī)用口罩抗人工合成血滲透的標(biāo)準(zhǔn)試驗(yàn)方法(已知速度下固定體積的水平投影)。 |
現(xiàn)行 |
2017 |
|
ASTM F2100-2019 |
醫(yī)用口罩材料性能標(biāo)準(zhǔn)規(guī)范。 |
現(xiàn)行 |
2019 |
|
|
ASTM F2101-2019 |
用金黃色葡萄球菌生物氣溶膠評價(jià)醫(yī)用口罩材料的細(xì)菌過濾效率(BFE)的標(biāo)準(zhǔn)試驗(yàn)方法。 |
現(xiàn)行 |
2019 |
|
|
ASTM F2299/F2299M-2003(2017) |
用膠乳球測定醫(yī)用面具材料粒子滲透性初始效率的標(biāo)準(zhǔn)試驗(yàn)方法。 |
現(xiàn)行 |
2003 |
|
|
澳大利亞 |
AS/NZS 1715:2009 |
呼吸保護(hù)設(shè)備的選擇,使用和維護(hù)。 |
現(xiàn)行 |
2009/2/6 |
|
AS/NZS 1716:2012 |
呼吸保護(hù)裝置。 |
現(xiàn)行 |
2012/2/13 |
|
|
日本 |
JIS T 8062:2010 |
預(yù)防傳染性病原體的防護(hù)服.面罩.防止人造血漿滲透的試驗(yàn)方法(確定容量,平行注射)。 |
現(xiàn)行 |
2010/5/25 |
|
JIS T 8159:2006 |
呼吸防護(hù)設(shè)備的選擇、使用和維護(hù)指南。 |
現(xiàn)行 |
2006/4/25 |
|
|
JIS T 8159:2006 |
呼吸保護(hù)裝置泄漏率試驗(yàn)方法。 |
現(xiàn)行 |
2006/2/20 |
|
|
韓國 |
KS M 6673-2008 |
防塵口罩 |
現(xiàn)行 |
2008/2/22 |
|
KS K ISO 22609-2018 |
傳染試劑防護(hù)服.醫(yī)療面罩.防人造血滲透的試驗(yàn)方法(固定容積、水平噴射)。 |
現(xiàn)行 |
2018/11/14 |
*以上技術(shù)標(biāo)準(zhǔn)如有動(dòng)態(tài)調(diào)整,以相關(guān)標(biāo)準(zhǔn)管理機(jī)構(gòu)官方發(fā)布為準(zhǔn)。







